Antimon
Antimon adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Sb dan nomor atom 51.
Fisik Antimon
Antimon merupakan unsur dengan warna putih keperakan, berbentuk kristal padat yang rapuh. Daya hantar listrik (konduktivitas) dan panasnya lemah. Zat ini menyublim (menguap dari fase padat) pada suhu rendah. Sebagai sebuah metaloid, antimon menyerupai logam dari penampilan fisiknya tetapi secara kimia ia bereaksi berbeda dari logam sejati.
Kegunaan Antimon Dalam Kehidupan Sehari-Hari
Antimon dimanfaatkan dalam produksi industri semikonduktor dalam produksi diode dan detektor infra merah. Sebagai sebuah campuran, logam semu ini meningkatkan kekuatan mekanik bahan. Manfaat yang paling penting dari antimon adalah sebagai penguat timbal untuk batere. Kegunaan-kegunaan lain adalah campuran antigores, korek api, obat-obatan dan pipa.
Oksida dan sulfida antimon, sodium antimonat, dan antimon triklorida digunakan dalam pembuatan senyawa tahan api, keramik, gelas, dan cat. Antimon sulfida alami (stibnit) diketahui telah digunakan sebagai obat-obatan dan kosmetika dalam masa Bibel.
Antimon dan senyawa-senyawanya adalah toksik (beracun). Secara klinis, gejala akibat keracunan antimon hampir mirip dengan keracunan arsen. Dalam dosis rendah, antimon menyebabkan sakit kepala dan depresi. Dalam dosis tinggi, antimon akan mengakibatkan kematian dalam beberapa hari.
Pada temperatur tinggi, antimon terkadang bisa mendai katalisator, membantu terurainya senyawa kimia menjadi unsur kimia asal terutama pada senyawa yang mempunyai relatif suhu leleh tinggi atau suhu nyala tinggi misalnya menguraikan thiner dari material anti gores pada cat logam atau menguraikan alkohol dari cairan rem atau minyak pelumas.

Senyawa Antimon
Antimon pentafluorida SbF5
Antimon trioksida Sb2O3
Antimon trihidrida SbH3 (stibina)
Indium antimonida (InSb)
Isotop Antimon
Isotop Antimont terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 121Sb | 57.36% | 121Sb stabil dengan 70 neutron | |||
| 123Sb | 42.64% | 123Sb stabil dengan 72 neutron | |||
| 125Sb | syn | 2.7582 y | β− | 125Te | |
Sejarah Antimon
Nama “antimon” berasal dari dua kata Yunani: ‘anti’ dan ‘monos’ yang berarti ‘tidak sendiri’. Nama itu diberikan karena antimon jarang ditemukan asli; Biasanya dikombinasikan dengan belerang atau dengan logam berat seperti tembaga, timbal dan perak.
Orang telah memanfaatkan senyawa antimon selama ribuan tahun. Kita tahu bahwa salah satu mineral antimon, stibnite(Sb2S3), digunakan dalam kosmetik Mesir empat atau lima ribu tahun yang lalu sebagai garis mata hitam.
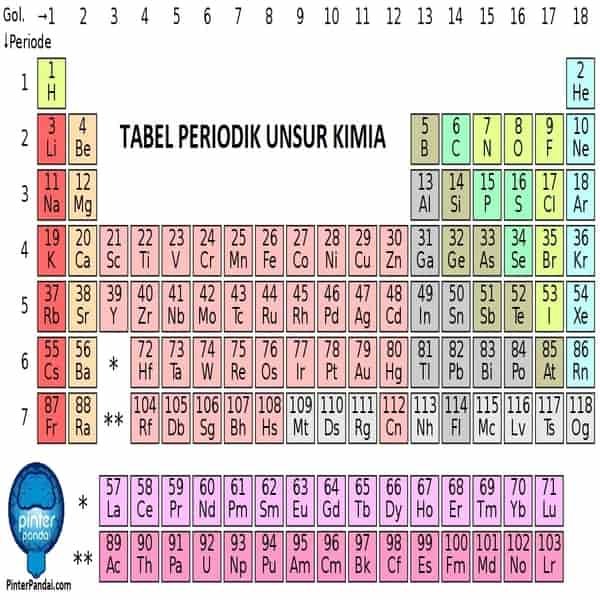
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Manfaat Emas Dalam Pengobatan Kesehatan Medis
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
Sumber bacaan: Royal Society of Chemistry, Study
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing