Perak
Perak adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Ag & nomor atom 47.
Ini adalah elemen yang paling reflektif dan juga memiliki konduktivitas listrik dan termal tertinggi dari logam manapun. Properti ini membuatnya sangat berguna untuk berbagai keperluan, mulai dari perhiasan dan peralatan hingga konduktor listrik, cermin dan panel surya. Senyawa perak digunakan dalam film fotografi, alat kesehatan dan desinfektan. Perak ditemukan di kerak bumi dalam bentuk aslinya, dicampur dengan logam lain dan mineral seperti argentit.
Kegunaan Perak Dalam Kehidupan Sehari-Hari
Contoh sederhananya saja perak digunakansebagai bahan dasar trofi kejuaraan, uang logam / koin dan perhiasan. Penggunaan perak dalam kehidupan dikarenakan warna kilau mengkilatnya yang menarik, lebih tahan korosi dan kelimpahannya di dunia. Selain itu, perak merupakan logam mulia yang harganya lebih terjangkau dibandingkan dua logammulia lain yaitu Platina (Pt) dan Emas (Au).
Perak digunakan dalam industri elektronik karena konduktivitas listrik yang sangat baik. Perak banyak digunakan dalam aplikasi berkualitas tinggi di mana logam tembaga tidak dapat melakukan pekerjaan. Perak juga digunakan dalam baterai.
Aplikasi lain untuk perak termasuk cermin, tambalan gigi, alat musik dan reaktor nuklir.

Fisik Perak
Sebuah logam transisi lunak, putih dan berkilau, ia memiliki konduktivitas listrik, konduktivitas termal dan reflektivitas tertinggi di antara semua logam. Logam ini terjadi secara alamiah dalam bentuk murni, bentuk bebas (perak asli), sebagai paduan dengan emas dan logam lainnya, dan dalam mineral seperti argentit dan klorargirit. Kebanyakan perak diproduksi sebagai produk samping penambangan tembaga, emas, timah dan seng.
Titik leleh perak adalah 961,5 ° C dan titik didihnya sekitar 2.000 sampai 2.200 ° C. Kepadatannya adalah 10,49 gram per sentimeter kubik.
Sifat Fisika Perak
| Fase: | padat |
|---|---|
| Titik lebur: | 1234,93 K (961,78 °C, 1763,2 °F) |
| Titik didih: | 2435 K (2162 °C, 3924 °F) |
| Kepadatanmendekati s.k.: | 10.49 g/cm3 |
| saat cair, pada t.l.: | 9.320 g/cm3 |
| Kalor peleburan: | 11,28 kJ/mol |
| Kalor penguapan: | 250,58 kJ/mol |
| Kapasitas kalor molar: | 25,350 J/(mol·K) |
Sifat Atom Perak
| Bilangan oksidasi: | 1, 2, 3 (oksida amfoter) |
|---|---|
| Elektronegativitas: | Skala Pauling: 1,93 |
| Jari-jari atom: | empiris: 144 pm |
| Jari-jari kovalen: | 145±5 pm |
| Jari-jari van der Waals: | 172 pm |
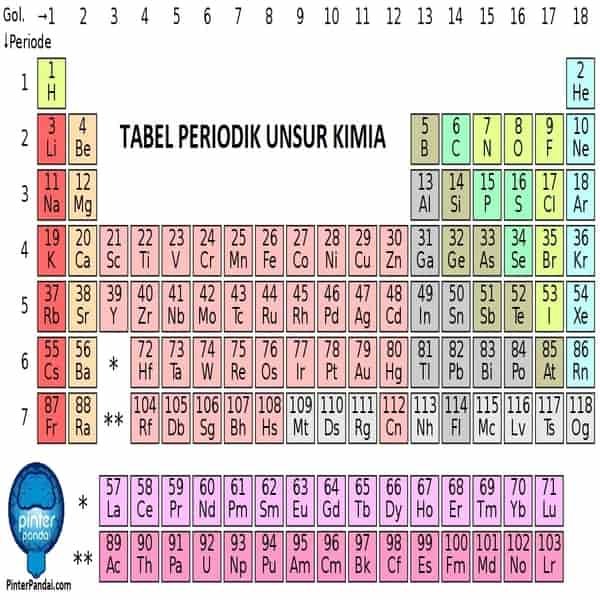
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Senyawa Perak
Logam perak mudah larut dalam asam nitrat (HNO3) menghasilkan perak nitrat (AgNO3), yang disebut ‘Kaustik Bulan’, suatu padatan kristal transparan yang bersifat fotosensitif dan mudah larut dalam air. Perak nitrat digunakan sebagai titik awal untuk sintesis banyak senyawa perak lainnya, sebagai antiseptik dan sebagai pewarna kuning untuk kaca pada kaca berwarna.
Logam perak ini tidak bereaksi dengan asam sulfat, yang digunakan dalam pembuatan perhiasan untuk membersihkan dan menghilangkan firescale tembaga oksida dari artikel perak setelah penyolderan perak atau annealing. Perak mudah bereaksi dengan belerang atau hidrogen sulfida H2S menghasilkan perak sulfida, suatu senyawa berwarna gelap seperti noda yang dijumpai pada koin perak dan objek lain. Perak sulfida Ag2S juga membentuk kumis perak ketika kontak listrik perak digunakan dalam atmosfer yang kaya akan hidrogen sulfida.
Perak klorida (AgCl)
Perak klorida (AgCl) diendapkan dari larutan perak nitrat dengan adanya ion klorida dan perak halida lainnya digunakan dalam pabrikasi emulsi fotografi yang dibuat dengan cara yang sama, menggunakan garam bromida atau iodida. Perak klorida digunakan dalam elektrode kaca untuk pengujian pH dan pengukuran potensiometri dan sebagai semen transparan untuk kaca. Perak iodida telah digunakan dalam percobaan penyemaian awan untuk menghasilkan hujan. Perak halida sangat sukar larut dalam larutan akuatik dan digunakan dalam metode analisis gravimetri.
Perak oksida (Ag2O), yang dihasilkan ketika larutan perak nitrat diberi perlakuan dengan basa, digunakan sebagai elektrode positif (anoda) dalam baterai arloji. Perak karbonat (Ag2CO3) mengendap ketika perak nitrat diberi perlakuan dengan asam karbonat (Na2CO3).
Perak fulminat (AgONC)
Perak fulminat (AgONC), adalah bahan peledak yang kuat dan peka sentuhan yang digunakan dalam topi perkusi dan dibuat dengan mereaksikan asam nitrat dengan asam nitrat dengan adanya etanol (C2H5OH). Senyawa perak lainnya yang berbahaya dan mudah meledak adalah perak azida (AgN3), dibuat dengan mereaksikan perak nitrat dengan natrium azida (NaN3) dan perak asetilida, terbentuk ketika perak bereaksi dengan gas asetilena.
Santir laten
Santir laten (bahasa Inggris: Latent image) yang terbentuk dalam kristal perak halida dikembangkan melalui perlakuan dengan reduktor, seperti hidrokuinon, mentol (4-(metilamino)fenol sulfat) atau askorbat dalam larutan alkalis, yang mereduksi halida terpapar pada logam perak.
Larutan alkalis perak nitrat dapat juga direduksi menjadi logam perak oleh gula pereduksi seperti glukosa, dan reaksi ini digunakan pada cermin kaca perak dan interior ornamen Natal dari kaca.
Perak halida mudah larut dalam larutan natrium tiosulfat (Na2S2O3), yang digunakan sebagai fikser fotografi, untuk menghilangkan kelebihan perak halida dari emulsi fotografi setelah pengembangan gambar.
Oksidasi logam perak
Logam perak dapat diserang oleh oksidator kuat seperti kalium permanganat (KMnO4) dan kalium dikromat (K2Cr2O7) dan dengan adanya kalium bromida (KBr); senyawa-senyawa ini digunakan dalam fotografi untuk mengelantang citra-citra perak, mengubahnya menjadi perak halida yang dapat difiksasi dengan tiosulfat maupun dikembangkan ulang untuk mengintensifkan citra originalnya. Perak membentuk kompleks sianida (perak sianida) yang larut dalam air dengan adanya kelebihan ion sianida. Larutan perak sianida digunakan dalam elektroplating perak.
Meskipun perak normalnya memiliki tingkat oksidasi +1 dalam senyawa, diketahui pula tingkat oksidasi lainnya, misalnya +3 dalam AgF3, yang dihasilkan dari reaksi unsur perak atau perak fluorida dengan kripton difluorida.
Artefak perak mengalami tiga bentuk deteriorasi, yang paling umum adalah korosi dengan pembentukan lapisan hitam perak sulfida. Perak klorida segar, terbentuk ketika objek perak dicelupkan dalam air garam untuk waktu lama, berwarna kuning pucat, menjadi keunguan di bawah paparan cahaya dan sedikit terproyeksi dari permukaan artefak atau koin. Pengendapan tembaga dalam perak antik dapat digunakan untuk mengetahui umur artefak.
Isotop Perak
Perak alami tersusun atas dua isotop stabil, 107Ag dan 109Ag, dengan 107Ag sedikit lebih melimpah (51.839% kelimpahan alami). Kelimpahan yang hampir sama jarang didapat dalam tabel periodik. Berat atom perak 107,8682(2) g/mol.
Sekitar 16 isotop radioaktif perak juga diketahui. Isotop radioaktif adalah salah satu yang pecah dan mengeluarkan beberapa bentuk radiasi. Isotop radioaktif dihasilkan saat partikel sangat kecil dipecat pada atom. Partikel ini menempel di atom dan membuatnya menjadi radioaktif.
Tak satu pun dari isotop radioaktif perak yang memiliki penggunaan komersial.
Isotop Perak terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 105Ag | syn | 41.2 d | ε | 105Pd | |
| γ | – | ||||
| 106mAg | syn | 8.28 d | ε | 106Pd | |
| γ | – | ||||
| 107Ag | 51.839% | 107Ag stabil dengan 60 neutron | |||
| 108mAg | syn | 418 y | ε | 108Pd | |
| IT | 108Ag | ||||
| γ | – | ||||
| 109Ag | 48.161% | 109Ag stabil dengan 62 neutron | |||
| 111Ag | syn | 7.45 d | β− | 111Cd | |
| γ | – | ||||
Sejarah Perak
Istilah silver muncul dalam bahasa Anglo-Saxon dengan ejaan yang beragam, seperti seolfor and siolfor. Perak adalah salah satu logam yang pertama kali ditemukan oleh orang-orang kuno. Artefak perak telah ditemukan di banyak peradaban kuno seperti Sumeria dari 3000 SM.

Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, Chemistry Explained
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing