Indium
Indium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang In dan nomor atom 49.
Ini adalah logam pasca transisi yang menyusun 0,21 ppm dari kerak bumi. Indium sangat lembut dan lunak, memiliki titik lebur lebih tinggi daripada natrium dan galium, tetapi lebih rendah daripada litium dan timah. Secara kimiawi, indium mirip dengan galium dan thallium, dan sebagian besar sifatnya berada di antara galium dan thallium.
Kegunaan Indium
Indium digunakan sebagai bahan campuran logam, campuran logam poros, transistor germanium, termistor dan fotokonduktor. Ia dapat dilapisi pada logam dan diuapkan pada gelas untuk membentuk kaca sebagus yang tebuat dari perak tetapi tidak rentan korosi atmosfir.
Indium timah oksida (ITO), oksida indium, banyak digunakan dalam pembuatan layar LCD. Sebenarnya, 50% logam ini digunakan dalam produksi display kristal cair.
Selain menjadi bagian penting dari layar komputer, LCD juga banyak digunakan di receiver GPS, kamera, PDA, mesin penjawab, telepon seluler, dan berbagai konfigurasi lainnya.
Karena meningkatnya permintaan di industri elektronik konsumen, harga logam ini telah melonjak ratusan dolar per kilogram.
Hal ini biasa digunakan pada komponen listrik seperti detektor inframerah, transistor kecepatan tinggi, dan perangkat foto-volta. Karena titik lebur yang rendah dan kemampuan untuk melakukan listrik, digunakan dalam pembuatan solder dan paduan.
Logam ini juga banyak digunakan dalam lapisan gelas. Meskipun pelapis semacam itu transparan, mereka mencerminkan sinar inframerah. Ini digunakan di jendela pesawat terbang, jendela arsitektur, pintu, lemari es, dan oven.
Timah oksida Indium populer digunakan pada lampu sodium bertekanan rendah. Dalam reaktor nuklir, neutron indium digunakan di batang kendali reaktor.
Di bidang kedokteran nuklir, indium leukocyte scintigraphy digunakan untuk memantau fungsi sel darah putih. Berikut adalah beberapa kegunaan elemen metalik ini:
Indium oksida dan timah oksida indium digunakan sebagai lapisan untuk panel electroluminescent.
Indium antimonide, indium phosphide, dan indium nitride adalah beberapa bahan semikonduktor yang populer di industri ini.
Elemen ini juga digunakan pada lampu LED dan dioda laser.
Ini digunakan sebagai paduan solder karena kemampuannya untuk mengisi perbedaan koefisien ekspansi termal (CTE) dari 2 logam berbeda, yang menyebabkan kerusakan pada sambungan logam, karena kontraksi dan ekspansi.
Bentuk Fisik
Indium adalah logam pasca transisi berwarna putih-keperakan yang sangat ulet dengan kilau terang. Ia sangat lembut (kekerasan Mohs 1,2) seperti natrium, dan bisa dipotong menggunakan pisau. Ia juga meninggalkan garis yang terlihat di atas kertas.

Sifat Fisika Indium
Fase: padat
Titik lebur: 429,7485 K (156,5985 °C, 313,8773 °F)
Titik didih: 2345 K (2072 °C, 3762 °F)
Kepadatan mendekati s.k.: 7,31 g/cm3
saat cair, pada t.l. 7,02 g/cm3
Titik tripel: 429,7445 K, ~1 kPa[1]
Kalor peleburan: 3,281 kJ/mol
Kalor penguapan: 231,8 kJ/mol
Kapasitas kalor molar: 26.74 J/(mol·K)
Sifat Atom Indium
Bilangan oksidasi: 3, 2, 1, −1, −2, −5 (suatu oksida amfoter)
Elektronegativitas Skala Pauling: 1,78
Energi ionisasi ke-1: 558,3 kJ/mol
ke-2: 1820,7 kJ/mol
ke-3: 2704 kJ/mol
Jari-jari atom empiris: 167 pm
Jari-jari kovalen: 142±5 pm
Jari-jari van der Waals: 193 pm
Sifat Kimia Indium
Indium memiliki 49 elektron, dengan konfigurasi elektron [Kr]4d105s25p1. Dalam senyawa, indium paling sering menyumbangkan tiga elektron terluarnya menjadi indium(III), In3+. Dalam beberapa kasus, pasangan elektron 5s tidak disumbangkan, menghasilkan indium(I), In+. Stabilisasi keadaan monovalen terkait dengan efek pasangan inert, di mana efek relativistik menstabilkan orbital 5s, yang teramati pada unsur yang lebih berat.
Sejumlah potensial elektroda standar indium yang dilaporkan, tergantung pada reaksi yang diteliti,[14] mencerminkan penurunan stabilitas tingkat oksidasi +3:
| −0,40 | In2+ + e− | ↔ In+ |
| −0,49 | In3+ + e− | ↔ In2+ |
| −0,443 | In3+ + 2 e− | ↔ In+ |
| −0,3382 | In3+ + 3 e− | ↔ In |
| −0,14 | In+ + e− | ↔ In |

Senyawa Indium
- Indium(I)
Senyawa indium(I) tidak umum. Klorida, bromida, dan iodidanya sangat berwarna, tidak seperti trihalida nya yang merupakan bahan bakunya. Fluoridanya dikenal sebagai senyawa gas yang tidak stabil. Bubuk hitam indium(I) oksida dihasilkan saat oksida indium(III) terdekomposisi pada pemanasan sampai 700 °C.
Indium(III)
- In(OH)3 + 3 HCl → InCl3 + 3 H2O
Diketahui juga seskuikalsogenida analognya dengan belerang, selenium dan telurium. Indium membentuk trihalida. Klorinasi, brominasi, dan iodinasi In menghasilkan InCl3dan InBr3 yang tak berwarna, serta InI3 yang berwarna kuning. Senyawanya merupakan asam Lewis, agak mirip dengan trihalida aluminium yang lebih dikenal. Sekali lagi seperti senyawa alumunium terkait, InF3 dapat membentuk polimer.
Reaksi langsung indium dengan pniktogen menghasilkan semikonduktor III-V yang berwarna abu-abu atau semimetalik. Banyak dari mereka perlahan terdekomposisi di udara lembab, sehingga penyimpanan senyawa semikonduktor secara hati-hati untuk mencegah kontak dengan atmosfer sangat diperlukan. Indium nitrida mudah diserang oleh asam maupun basa.
- Tingkat oksidasi lain
Kadang-kadang, indium membentuk senyawa dengan tingkat oksidasi +2 dan bahkan tingkat oksidasi fraksional. Biasanya materials semacam itu memiliki ikatan In-In, terutama pada halida In2X4 dan [In2X6]2− dan berbagai subkalkogenida seperti In4Se3.
Beberapa senyawa lain diketahui merupakan kombinasi antara indium(I) dan indium(III), seperti InI6(InIIICl6)Cl3, InI5(InIIIBr4)2(InIIIBr6), InIInIIIBr4.
- Senyawa organoindium
Senyawa organoindium memiliki ikatan In–C. Sebagian besar merupakan turunan In(III), tetapi ada perkecualian yaitu siklopentadienilindium(I). Ini merupakan senyawa organoindium(I) yang pertama kali diketahui dan dapat bersifat polimerik, dengan rantai zigzag dan berseling antara atom indium dan kompleks siklopentadienil.
Kemungkinan, senyawa organoindium yang paling terkenal adalah trimetilindium, In(CH3)3, yang digunakan untuk membuat bahan semikondukter tertentu.
Isotop Indium
Indium memiliki 39 isotop yang diketahui, dengan rentang nomor massa antara 97 sampai 135. Hanya dua isotop yang terjadi secara alami sebagai nuklida purba: indium-113, satu-satunya isotop stabil, dan indium-115, yang memiliki waktu paruh 4,41×1014 tahun, empat orde besarnya lebih besar daripada umur alam semesta dan hampir 50.000 kali lebih besar daripada thorium alami.
Waktu paruh 115In sangat lama karena peluruhan beta menjadi 115Sn adalah spin-terlarang. Indium-115 menyusun 95,7% dari total indium. Indium adalah satu dari tiga unsur yang diketahui (yang lain adalah telurium dan renium) di mana isotop stabil kurang berlimpah di alam daripada radioisotop primordial berumur panjang.
Isotop Indium terstabil
| Isotop | Kelimpahan | Waktu paruh (t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 113In | 4,28% | 113In stabil dengan 64 neutron | |||
| 115In | 95,72% | 4,41×1014 y | β− | 115Sn | |
Sejarah Indium
Indium ditemukan pada tahun 1863 oleh Ferdinand Reichdan Hieronim Theodor Richter dengan metode spektroskopi. Mereka menamainya sesuai garis indigo dalam spektrumnya.

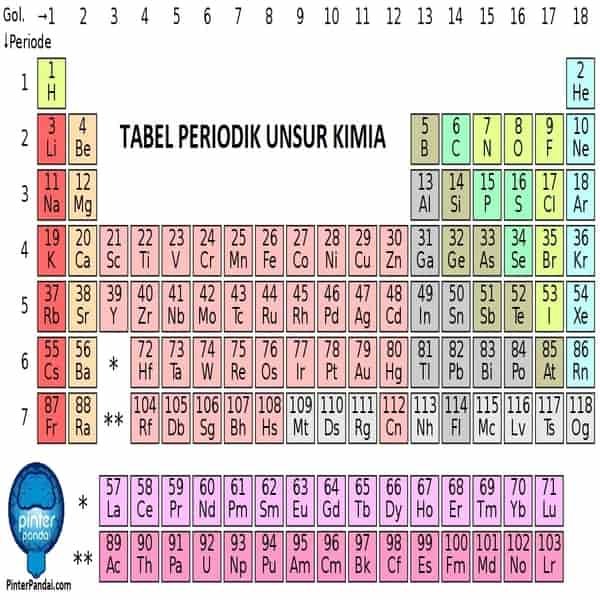
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, ChemSpider, Mindat.org
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya