Kripton
Kripton adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Kr dan nomor atom 36.
Kripton bukan hanya elemen yang membuat Superman menjadi lemah. Kripton adalah elemen aktual pada grafik dan bahkan di udara yang kita hirup. Ini dalam jumlah sangat kecil – sekitar 1 bagian per juta – tapi masih ada di sana… Di Mars, kripton juga ada dalam jumlah yang jauh lebih kecil sekitar 0,3 bagian per juta.
Fisik Kripton
Kripton ditandai oleh beberapa garis emisi yang tajam (seperti tanda tangan spektral) yang terkuat berwarna hijau dan kuning. Kripton adalah salah satu produk fisi uranium. Berbentuk padat berwarna putih dan memiliki struktur kristal kubik berpusat muka, yang merupakan milik umum semua gas mulia (kecuali helium, yang memiliki struktur kristal dekat heksagonal).

Kegunaan Kripton Dalam Kehidupan Sehari-Hari
Tingginya biaya memperoleh kripton dari udara telah membatasi benda-benda yang praktis untuk digunakan dalam kehidupan sehari-hari. Kripton digunakan dalam beberapa jenis “fotografi berkedip” yang digunakan dalam fotografi kecepatan tinggi. Kripton digunakan dalam lampu listrik dan neon tertentu dan dalam flashlamp digunakan dalam fotografi kecepatan tinggi.
Beberapa lampu neon yang diisi dengan campuran kripton dan gas argon. Gas kripton juga dikombinasikan dengan gas-gas lain untuk membuat tanda-tanda bercahaya yang bersinar dengan cahaya kehijauan-kuning. Pada tahun 1960, panjang meter didefinisikan dalam hal oranye-merah garis spektral kripton-86, sebuah isotop krypton.
Pernah dianggap benar-benar inert, kripton dikenal untuk membentuk beberapa senyawa. Kripton difluoride (KrF2) adalah senyawa kripton termudah untuk membuat dan jumlah gram itu telah diproduksi.
Sejarah Kripton
Ditemukan di Inggris pada pada tanggal 30 Mei 1898 oleh Sir William Ramsay, seorang ahli kimia Skotlandia dan Morris Travers, seorang ahli kimia Inggris, di dalam residu yang tersisa dari penguapan hampir semua komponen udara cair. Neon ditemukan oleh prosedur serupa oleh pekerja yang sama beberapa minggu kemudian.
William Ramsay dianugerahi Penghargaan Nobel Kimia 1904 untuk penemuan serangkaian gas mulia, termasuk krypton. Atmosfer bumi adalah sekitar 0,0001% kripton.
Sifat Elemen Kripton
Karena titik didihnya (-152,3 ° C, atau -242,1 ° F) adalah sekitar 30-40 ° C (50-70 ° F) lebih tinggi daripada unsur dari konstituen utama udara, kripton ini mudah dipisahkan dari udara cair dengan distilasi fraksional ; terakumulasi seiring dengan xenon dalam sedikit porsi volatil. Kedua gas tersebut selanjutnya dimurnikan dengan adsorpsi ke silika gel, redistillation, dan bagian atas logam titanium panas, yang menghilangkan semua kotoran kecuali gas mulia lainnya.
Senyawa Kripton
Kripton adalah unsur yang paling ringan dari gas mulia yang membentuk senyawa kimia isolable dalam jumlah makroskopik. Selama bertahun-tahun kripton dianggap benar-benar tidak reaktif. Akan tetapi pada awal 1960-an, kripton ditemukan bereaksi dengan elemen fluorin ketika keduanya digabungkan dalam sebuah tabung listrik-discharge pada -183 ° C (-297 ° F); senyawa yang terbentuk adalah krypton difluoride, KrF2. Beberapa metode lain untuk sintesis KrF2 yang sekarang dikenal, termasuk iradiasi campuran kripton dan fluor dengan radiasi ultraviolet pada -196 ° C (-321 ° F).
KrF2
KrF2 adalah kristal berwarna solid yang sangat volatile dan perlahan-lahan terurai pada suhu kamar. Tidak ada molekul kripton fluoride lain yang telah diisolasi, sehingga semua senyawa kripton berasal dari KrF2, di mana Kr dalam keadaan oksidasi +2. Kripton difluoride adalah agen fluorinating oksidatif kuat. (Daya pengoksidasi berarti bahwa senyawa ini mengekstrak elektron dari zat lain dan menganugerahkan mereka muatan positif. Kemampuan fluorinating berarti bahwa mereka mentransfer ion F untuk zat-zat lain. Oleh karena itu, dalam arti formal, fluorination oksidatif adalah hasil bersih dari ekstraksi dari dua elektron dan penambahan F, ini dapat dianggap setara dengan transfer F +) KrF2, misalnya, mampu mengoksidasi dan fluorinating xenon menjadi XeF6 dan emas untuk AuF5.
Spesies kationik KrF + dan Kr2F3 + terbentuk dalam reaksi KrF2 dengan akseptor fluoride-ion yang kuat seperti pentafluorides Grup 15, di mana ion F fluoride ditransfer ke pentafluoride untuk memberikan garam kompleks yang beranalog dengan unsur dari XeF2; di sini tidak ada oksidasi terlibat. Di antaranya garam kompleks [KrF +] [SbF6–] dan [Kr2F3 +] [AsF6–]. The Kr2F3 + kation berbentuk V dengan atom fluorin terikat pada masing-masing dua atom kripton dan kedua atom kripton terikat pada fluor di tengah, yaitu, F (KrF) 2+.
Kation KrF +
Kation KrF + menduduki tempat di antara oksidasi kimia yang paling kuat saat ini dikenal dan mampu melakukan fluorination oksidatif gas xenon untuk berubah menjadi XeF5 + dan klorin, bromin, dan iodin pentafluorides masing-masing ke ClF6 +, BrF6 +, dan kation IF6 +. Kation KrF + berperilaku hanya sebagai agen pengoksidasi dalam mengkonversi gas oksigen ke O2 +.
Kation KrF + telah terbukti berperilaku sebagai asam Lewis (pasangan elektron akseptor) terhadap sejumlah basa Lewis yang tahan terhadap oksidasi oleh pengoksidasi kuat kation KrF + pada suhu rendah. Adisi asam-basa Lewis ini yang dicontohkan oleh HCNKrF + dan F3CCNKrF +, yang terbentuk sebagai garam AsF6–. Kation tersebut adalah satu-satunya contoh yang dikenal dari kripton yang terikat pada nitrogen. Senyawa Kr (OTeF5) 2 adalah satu-satunya yang dilaporkan sebagai contoh senyawa kripton yang terikat pada oksigen. Tidak ada senyawa kripton yang terikat pada unsur-unsur lain dari fluor, oksigen, dan nitrogen yang telah diisolasi.
Klatrat “senyawa,” di mana unsur ini terjebak dalam struktur air cagelike atau molekul lain yang dikenal. Tidak ada molekul diatomik dari kripton.

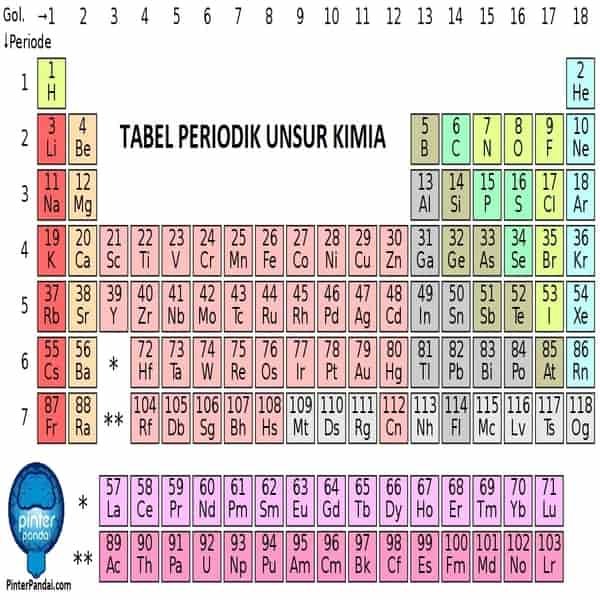
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Efek kesehatan kripton
Inhalasi: Gas ini inert dan diklasifikasikan sebagai asfiksia sederhana. Menghirup dalam konsentrasi yang berlebihan dapat menyebabkan pusing, mual, muntah, tidak sadarkan diri, dan kematian. Kematian dapat terjadi karena kesalahan dalam penilaian, kebingungan, atau hilangnya kesadaran individu yang datang untuk membantu orang lain. Pada konsentrasi oksigen rendah, ketidaksadaran dan kematian dapat terjadi dalam hitungan detik tanpa peringatan.
Efek gas sesak napas tunggal sebanding dengan tingkat penurunan jumlah (tekanan parsial) oksigen di udara yang dihirup. Oksigen dapat dikurangi hingga 75% dari persentase normal di udara sebelum gejala yang berarti berkembang. Alternatif ini membutuhkan adanya asfiksia sederhana dalam konsentrasi 33% dalam campuran udara dan gas. Ketika asfiksia sederhana mencapai konsentrasi 50%, gejala yang nyata dapat dihasilkan. Konsentrasi 75% berakibat fatal dalam beberapa menit.
Gejala: Gejala pertama yang ditimbulkan oleh asfiksia sederhana adalah pernapasan cepat dan terengah-engah. Kewaspadaan mental berkurang dan koordinasi otot terganggu. Penilaian posterior menjadi rusak dan semua sensasi berkurang. Ketidakstabilan emosi sering terjadi dan kelelahan terjadi dengan cepat. Saat asfiksia berlanjut, mungkin ada mual dan muntah, sujud dan kehilangan kesadaran, dan akhirnya kejang, koma dalam dan kematian.
Efek kripton pada lingkungan
Krypton adalah gas atmosfer yang langka, tidak beracun, dan inert secara kimia. Suhu dingin yang ekstrim (-244 o C) akan membekukan organisme saat kontak, tetapi tidak ada efek ekologi jangka panjang yang diharapkan.
Pertimbangan Pembuangan: Tidak memiliki sisa gas dalam tabung gas terkompresi. Kembalikan silinder ke pemasok dengan tekanan sisa, katup silinder tertutup rapat. Perhatikan persyaratan negara bagian dan lokal untuk pembuangan limbah yang mungkin lebih ketat atau berbeda dari peraturan federal. Konsultasikan peraturan negara bagian dan lokal mengenai pembuangan yang tepat dari bahan ini.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing