Paladium
Paladium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Pd dan nomor atom 46.
Bentuk Fisik
Merupakan logam langka berwarna putih berkilau keperakan.
Penggunaan Paladium

Sifat Fisika
Fase: padat
Titik lebur: 1828,05 K (1554,9 °C, 2830,82 °F)
Titik didih: 3236 K (2963 °C, 5365 °F)
Kepadatan mendekati s.k.: 12,023 g/cm3
saat cair, pada t.l.: 10,38 g/cm3
Kalor peleburan: 16,74 kJ/mol
Kalor penguapan: 362 kJ/mol
Kapasitas kalor molar: 25,98 J/(mol·K)
Sifat Atom Paladium
Bilangan oksidasi: 0, +1, +2, +4, +6 (sedikit oksida basa)
Elektronegativitas Skala Pauling: 2,20
Jari-jari atom empiris: 137 pm
Jari-jari kovalen: 139±6 pm
Jari-jari van der Waals: 163 pm
Senyawa Paladium
Paladium tidak bereaksi dengan oksigen pada temperatur normal (maka tidak memudar di udara). Paladium yang dipanaskan hingga 800 °C akan menghasilkan lapisan paladium(II) oksida (PdO). Ia sedikit memudar pada udara lembab yang mengandung belerang.[12]Paladium utama berada dalam tingkat oksidasi 0, +2, dan +4; meskipun tingkat oksidasi +4 langka. Satu contoh paladium(IV) adalah heksakloropaladat(IV), [PdCl6]2−.
Unsur paladium bereaksi dengan klorin menghasilkan paladium(II) klorida; yang larut dalam asam nitrat dan mengendap sebagai paladium(II) asetat pada penambahan asam asetat. Kedua senyawa ini dan bromidanya bersifat reaktif dan relatif murah, menjadikan mereka titik tolak yang sesuai menuju kimia paladium. Ketiganya bukan monomer; klorida dan bromida sering harus direfluks dalam asetonitril untuk mendapatkan monomer kompleks asetonitril yang lebih reaktif, misalnya:



Reduksi kompleks fosfin ini dengan hidrazin dan fosfin berlebih menghasilkan tetrakis(trifenilfosfin)paladium(0), salah satu dari dua kompleks paladium(0) utama:

Kompleks paladium valensi campuran Pd4(CO)4(OAc)4Pd(acac)2 membentuk struktur rantai Pd tak terhingga, dengan interkoneksi alternatif pada unit Pd4(CO)4(OAc)4 and Pd(acac)2.
Reaksi-reaksi yang melibatkan senyawa paladium sebagai katalis dikenal sebagai kumpulan reaksi penggandengan dikatalisis paladium. Contoh penting antar lain reaksi Heck, Suzuki dan Stille. Paladium(II) asetat, tetrakis(trifenilfosfin)paladium(0) (Pd(PPh3)4), dan tris(dibenzelidenaseton)dipaladium(0) (Pd2(dba)3) merupakan senyawa yang berguna, baik sebagai katalis maupun sebagai titik tolak katalis.
Isotop Paladium
Paladium alami terdiri dari tujuh isotop, enam di antaranya merupakan isotop stabil. Radioisotop paling stabil adalah 107Pd dengan waktu paruh 6,5 juta tahun (dijumpai di alam), 103Pd dengan waktu paruh 17 hari, dan 100Pd dengan waktu paruh 3,63 hari. Delapanbelas radioisotop lainnya berhasil diidentifikasi dengan massa atom berkisar antara 90,94948(64) u (91Pd) sampai 122,93426(64) u (123Pd).
Sebagian besar mempunyai waktu paruh kurang dari tigapuluh menit, kecuali 101Pd (waktu paruh: 8,47 jam), 109Pd (waktu paruh: 13,7 jam), dan 112Pd (waktu paruh: 21 jam).
Isotop Paladium terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 100Pd | syn | 3.63 d | ε | 100Rh | |
| γ | – | ||||
| 102Pd | 1.02% | 102Pd stabil dengan 56 neutron | |||
| 103Pd | syn | 16.991 d | ε | 103Rh | |
| 104Pd | 11.14% | 104Pd stabil dengan 58 neutron | |||
| 105Pd | 22.33% | 105Pd stabil dengan 59 neutron | |||
| 106Pd | 27.33% | 106Pd stabil dengan 60 neutron | |||
| 107Pd | renik | 6.5×106 y | β− | 107Ag | |
| 108Pd | 26.46% | 108Pd stabil dengan 62 neutron | |||
| 110Pd | 11.72% | 110Pd stabil dengan 64 neutron | |||
Sejarah Paladium
William Hyde Wollaston mencatat penemuan logam mulia baru pada Juli 1802 dalam buku laboratoriumnya dan menamakannya paladium pada bulan Agustus tahun yang sama. Wollaston memurnikan material itu secukupnya dan menawarkannya, tanpa menyebut penemunya, di sebuah toko kecil di Soho pada bulan April 1803.
Setelah kritik keras yang dilontarkan oleh Richard Chevenix bahwa paladium merupakan paduan platina dan raksa, Wollaston secara anonim menawarkan hadiah 20 poundsterling untuk 20 butir paduanpaladium sintetis.
Chevenix menerima Medali Copley pada tahun 1803 setelah ia menerbitkan percobaan pada paladium. Wollaston menerbitkan penemuan rodium pada tahun 1804 dan menyebutkan beberapa karyanya pada paladium. Dia mengungkapkan bahwa ia adalah penemu dari paladium dalam suatu publikasi pada tahun 1805.

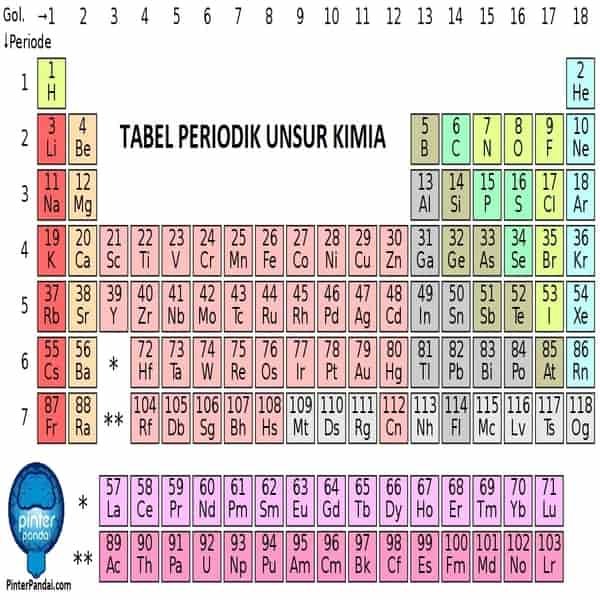
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, Chemistry Explained
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya