Vanadium
Vanadium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang V dan nomor atom 23.
Penggunaan Vadium
- Untuk membuat peralatan yang membutuhkan kekuatan dan kelenturan yang tinggi seperti per mobil dan alat mesin berkecepatan tinggi,
- Oksida vanadium (V2O5) digunakan sebagai katalis dalam pembuatan asam sulfat dengan proses kontak.
- Untuk membuat logam campuran.
- Umumnya digunakan untuk paduan dengan logam lain seperti baja tahan karat dan baja untuk peralatan berat karena sifatnya merupakan logam putih terang, relatif lunak dan liat, tahan terhadap korosif, asam, basa dan air garam.
- J.2.5. V2O5digunakan sebagai katalis pada proses pembuatan asam sulfat dan digunakan sebagai reduktor.
- Foil vanadium digunakan sebagai zat pengikat dalam melapisi titanium pada baja.
- Vanadium petoksida digunakan dalam pembuatan keramik dan sebagai katalis.
- Vanadium juga digunakan untuk menghasilkan magnet superkonduktif dengan medan magnet sebesar 175000 Gauss.
Bentuk Fisik Vanadium
Salah satu senyawa yang mengandung vanadium antara lain vanadium pentaoksida (V2O5).Vanadium juga merupakan Logam mulia yang cukup keras, Logam ini hanya bisa ditemukan di tempat-tempat tertentu.
Vanadium mempunyai kekuatan struktur yang baik dan keratin rentas belahan neutron yang rendah, menyebabkannya berguna dalam aplikasi nuklir. Walaupun ia sejenis logam, vanadium bersama dengan kromium dan mangan mempunyai cirri-ciri oksida valensi yang bersifat asid.

Sifat Fisika Vanadium
Fase: solid
Titik lebur: 2183 K (1910 °C, 3470 °F)
Titik didih: 3680 K (3407 °C, 6165 °F)
Kepadatan mendekati s.k.: 6.0 g/cm3
saat cair, pada t.l.: 5.5 g/cm3
Kalor peleburan: 21.5 kJ/mol
Kalor penguapan: 459 kJ/mol
Kapasitas kalor molar: 24.89 J/(mol·K)
Sifat Atom Vanadium
Bilangan oksidasi: 5, 4, 3, 2, 1, -1 oksida amfoter
Elektronegativitas Skala Pauling: 1.63
Energi ionisasi
Jari-jari atom empiris: 134 pm
Jari-jari kovalen: 153±8 pm

Senyawa Vanadium
Senyawa V⁺⁵
Vanadium Pentoksida, V₂O₅,
Oksidasi/pemanggangan logam atau oksidanya dengan bilangan oksidasi rendah. V₂O₅ sebagai hasil akhir. Hidrolisa VOCI₃ pemanasan amonium vanadate penggunaan :
Sebagai katalis dalam oksidasi SO₂SO₃, dalam pembuatan asam sulfat V₂O₅2SO₂+O₂2SO₃ Katalis dalam oksidasi alkohol dan hidrogenasi olefin.
Senyawa V⁺⁴
Vanadium titroksida,V₂O₄ atau VO₂. Dibuat dengan pemanasan campuran vanadium trioksida dan vanadium pentoksida tanpa udara dengan jumlah molar yang sama. Senyawa ini berbentuk Kristal biru tua, mudah larut dalam asam atau basa.
Vanadium titra flourida, VF₄. Dibuat dari reaksi HF anhirid dengan VCl₄. Reaksi berjalan mulai suhu -28 °C dan meningkat secara lambat sampai 0°C. Fluorida ini berupa bubuk kuning kecoklatan, larut dalam air membentuk larutan berwarna biru.
Senyawa Vanadil, senyawa ini berisi kation vanadil (VO+2) dimana bilangan oksidasinya +4, bersifat unik, berwarna biru. Vanadil klorida dibuat dari hidrolisaVCl₄+ H₂O→VOC₁₂+2HCIatau dari reaksi V₂O₅ dengan HCIV₂O₅+ HCI→2VOCI₂+3H₂O+CI₂ Senyawa VOCI₂ bersifat reduktor kuat yang digunakan secara komersial dalam pewarnaan. Hanya E₀ dari VO+2/VO3 adalah-1Volt.
Senyawa V⁺3
Vanadium trioksida, V₂O₃. Dibuat dengan mereduksi V₂O₅dengan hydrogen. V₂O₃ bersifat basa, larut dalam asam memberikan ion hezaquo, V(H₂O)63+.
Vanadium halida dan oxihalida. Vanadium triflourida, VF₃. 3H₂O dibuat bila V₂O₃ dilarutkan dalam HF. Trihalida yang lain adalah VCI₃ dan VBr₃, sedang VI₃ tidak dikenal. Vanadium oxihalida yang dikenal adalah VOCI dan VOBr. Keduanya tak larut dalam air tetapi larut dalam asam.
Senyawa V+2
Senyawa-senyawa V+2 berwarna paramagnetic ion V+2merupakan reduktor kuat. Larutan encer V+2 (violet) mereduksi air membebaskan H2V+2H→V+3+½H2.Senyawa V+1, dan V-1 dan V0.Bilangan oksidasi ini tidak umum, distabilkan oleh ligan asam n. Bilangan oksidasi +1 dijumpai pada senyawa V(C2)6-1
Isotop Vanadium
Isotop Vanadium terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk |
|---|---|---|---|---|
| 48V | syn | 15.9735 d | ε+β+ | 48Ti |
| 49V | syn | 330 d | ε | 49Ti |
| 50V | 0.25% | 1.5×1017tahun | ε | 50Ti |
| β− | 50Cr |

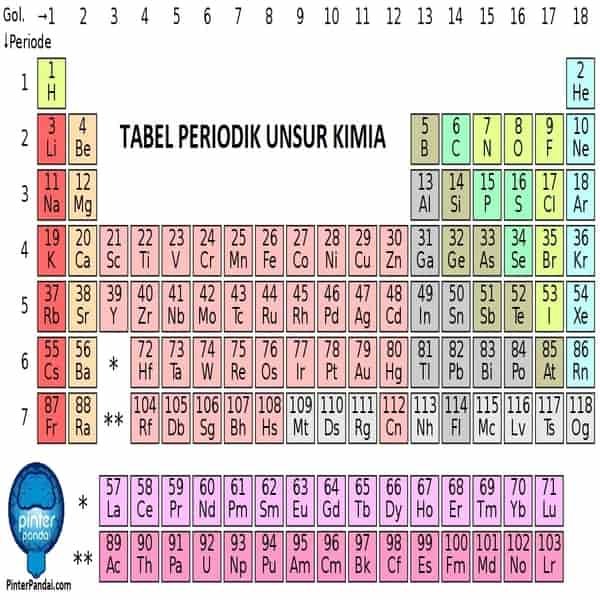
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Simbol Fisika dan Kimia | Arti Lambang dan Penjelasan
- hbar memainkan peran sentral dalam fisika mekanika kuantum (H Coret)
- Reaktor Nuklir Alami Zaman Purba
- Kebiri Kimia (kastrasi kimia) | Penjelasan, Tujuan dan Efek
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, Images of Elements, National Center for Biotechnology Information, U.S. National Library of Medicine
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing