Pengertian Barium Adalah
Barium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Ba dan nomor atom 56.
Barium adalah unsur kelima pada golongan 2 dan merupakan logam alkali tanah yang lunak dan keperakan. Barium tidak pernah ditemukan di alam sebagai unsur bebas karena reaktivitas kimianya yang tinggi. Hidroksidanya, yang dikenal dalam sejarah pra-modern sebagai barita, tidak terjadi sebagai mineral, namun dapat dibuat dengan memanaskan barium karbonat.
Mineral barium adalah mineral alami yang paling umum terjadi adalah barit (barium sulfat, BaSO4) dan witerit (barium karbonat, BaCO3), keduanya tidak larut dalam air. Nama barium berasal dari turunan alkimia “baryta”, dari bahasa Yunani: βαρύς (barys), yang berarti “berat.” Barik adalah bentuk ajektif dari barium. Barium diidentifikasi sebagai unsur baru pada tahun 1774, namun baru direduksi menjadi logamnya pada tahun 1808 dengan munculnya elektrolisis.
Penggunaan Barium
Barium memiliki beberapa aplikasi industri. Secara historis, itu digunakan sebagai penangkap untuk tabung vakum. Ia adalah komponen dari YBCO (superkonduktor suhu tinggi) dan elektrokeramik, dan ditambahkan ke baja dan besi tuang untuk mengurangi ukuran butiran karbon di dalam struktur mikro. Senyawanya ditambahkan ke dalam kembang api untuk memberikan warna hijau.
Barium sulfat digunakan sebagai aditif yang tidak larut pada fluida pengeboran sumur minyak, dan juga dalam bentuk yang lebih murni, seperti zat radiokontras sinar-X untuk pencitraan sistem pencernaan manusia.
Ion dan senyawa barium terlarut adalah beracun, dan telah digunakan sebagai rodentisida.
Sifat Fisika Barium
Ini adalah logam lunak putih keperakan, dengan sedikit nuansa emas saat ultra murni. Warna putih keperakan logam barium dengan cepat menghilang pada oksidasi di udara, menghasilkan lapisan oksida abu-abu gelap. Barium memiliki bobot jenis menengah dan merupakan konduktor listrik yang baik. Barium ultra murni sangat sulit disiapkan, dan oleh karena itu banyak sifat barium belum ditentukan secara akurat.
Pada suhu dan tekanan ruangan, barium memiliki struktur kubik berpusat pada tubuh, dengan jarak barium–barium 503 pikometer, mengembang dengan pemanasan pada laju sekitar 1,8×10-5/°C. Ini adalah logam yang sangat lunak dengan kekerasan Mohs 1,25.
Titik lelehnya 1000 K (730 °C; 1340 °F) berada di antara unsur stronsium yang lebih ringan (1050 K or 780 °C or 1430 °F) dan radium yang lebih berat (973 K or 700 °C or 1292 °F); namun, titik didihnya 2170 K (1900 °C; 3450 °F) melampaui stronsium (1655 K or 1382 °C or 2519 °F). Massa jenisnya (3,62 g·cm−3) lagi-lagi berada di antara stronsium (2,36 g·cm−3) dan radium (~5 g·cm−3).
Reaktivitas kimia
Secara kimiawi mirip dengan magnesium, kalsium, dan stronsium, namun lebih reaktif. Barium selalu menunjukkan tingkat oksidasi +2, kecuali beberapa spesies molekuler langka dan tidak stabil yang hanya tercirikan dalam fase gas seperti BaF.
Reaksi dengan kalkogen sangat eksotermal (melepas energi); reaksi dengan oksigen atau udara terjadi pada suhu kamar, dan karena itu barium disimpan di dalam minyak atau atmosfir inert.
Reaksi dengan nonlogam lainnya, seperti karbon, nitrogen, fosfor, silikon, dan hidrogen, umumnya bersifat eksotermal dan berlanjut pada pemanasan. Reaksi dengan air dan alkohol sangat eksotermal dan melepaskan gas hidrogen:
Barium bereaksi dengan amonia untuk membentuk kompleks seperti Ba(NH)63.
Logam ini mudah diserang oleh kebanyakan asam. Asam sulfat adalah pengecualian karena pasivasi menghentikan reaksi dengan membentuk barium sulfat yang tidak larut di permukaan. Barium berpadu dengan beberapa logam, termasuk aluminium, seng, timbal, dan timah, membentuk intermetalik dan paduan.
Senyawa
| O2− | S2− | F− | Cl− | SO2−4 | CO2−3 | O2−2 | H− | |
|---|---|---|---|---|---|---|---|---|
| Ca2+ | 3,34 | 2,59 | 3,18 | 2,15 | 2,96 | 2,83 | 2,9 | 1,7 |
| Sr2+ | 5,1 | 3,7 | 4,24 | 3,05 | 3,96 | 3,5 | 4,78 | 3,26 |
| Ba2+ | 5,72 | 4,3 | 4,89 | 3,89 | 4,49 | 4,29 | 4,96 | 4,16 |
| Zn2+ | 5,6 | 4,09 | 4,95 | 2,09 | 3,54 | 4,4 | 1,57 | — |
Garam barium biasanya berwarna putih bila padat dan tidak berwarna saat dilarutkan, dan ion barium tidak memberikan pewarnaan tertentu.Mereka lebih padat daripada analog stronsiumatau kalsium, kecuali halida (lihat tabel; seng dicantumkan untuk perbandingan).
Barium hidroksida (“baryta”) dikenal oleh alkimiawan, yang memproduksinya dengan memanaskan barium karbonat. Tidak seperti kalsium hidroksida, ia menyerap sedikit CO2 dalam larutan akuatik dan oleh karena itu tidak peka terhadap fluktuasi atmosfer. Sifat ini digunakan untuk mengkalibrasi peralatan pH.
Senyawa barium volatil terbakar dengan nyala hijau sampai hijau pucat, yang merupakan pebgujian yang efisien untuk mendeteksi senyawa barium. Warna dihasilkan dari garis spektral pada 455,4, 493,4, 553,6, dan 611,1 nm.
Senyawa organobarium adalah bidang pengetahuan yang berkembang: penemuan saat ini adalah dialkilbarium dan alkilhalobarium.

Isotop Barium
Barium yang ditemukan di kerak bumi adalah campuran dari tujuh nuklida primordial, barium-130, 132, dan 134 sampai 138. Barium-130 mengalami peluruhan radioaktif yang sangat lambat menjadi xenon-130 melalui peluruhan beta plus berganda, dan barium-132 yang secara teoretis meluruh seperti xenon-132, dengan waktu paruh seribu kali lebih lama daripada usia alam semesta.
Kelimpahannya adalah ~ 0,1% dari barium alami.
Radioaktivitas isotop ini sangat lemah sehingga tidak menimbulkan bahaya bagi kehidupan.
Dari isotop stabil, barium-138 menyusun 71,7% dari semua barium, dan semakin ringan isotopnya, semakin kurang melimpah.
Secara total, barium memiliki sekitar 50 isotop yang diketahui, dengan kisaran massa antara 114 dan 153. Isotop metastabil yang paling stabil adalah barium-133 dengan waktu paruh sekitar 10,51 tahun. Lima isotop lain memiliki waktu paruh lebih dari satu hari. Barium juga memiliki 10 isomer nuklir, dari situ barium-133m1 adalah yang paling stabil dengan waktu paruh sekitar 39 jam.
| Isotop barium terstabil | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Sejarah Barium
Alkimiawan pada awal Abad Pertengahan mengetahui tentang beberapa mineral barium. Batu seperti kerikil yang halus mineral barit yang ditemukan di Bologna, Italia, dikenal sebagai “batu Bologna.” Alkimiawan tertarik padanya karena setelah terpapar cahaya mereka akan berpendar selama bertahun-tahun. Sifat fosforesen dari barit yang dipanaskan dengan bahan organik dijelaskan oleh V. Casciorolus pada tahun 1602.
Carl Scheele menentukan bahwa barit mengandung unsur baru pada tahun 1774, namun tidak dapat mengisolasi barium, hanya barium oksida. Johan Gottlieb Gahn juga mengisolasi barium oksida dua tahun kemudian dalam studi serupa. Barium teroksidasi pada awalnya disebut “barote” oleh Guyton de Morveau, sebuah nama yang diubah oleh Antoine Lavoisier menjadi baryta. Selain itu pada abad ke-18, ahli mineralogi Inggris William Withering mencatat mineral berat di tambang timbal Cumberland, yang sekarang dikenal sebagai witerit. Barium pertama kali diisolasi dengan cara elektrolisis garam barium cair pada tahun 1808 oleh Sir Humphry Davy di Inggris.
Davy, analog dengan kalsium, memberi nama “barium” dari nama baryta, dengan ujung “-ium” yang menandakan unsur logam.
Robert Bunsen dan Augustus Matthiessen memperoleh barium murni dengan elektrolisis cairan campuran barium klorida dan amonium klorida.
Produksi oksigen murni dalam proses proses Brin adalah aplikasi besar barium peroksida pada tahun 1880-an, sebelum digantikan oleh elektrolisis dan distilasi fraksi udara cair pada awal 1900-an. Dalam proses ini, barium oksida bereaksi pada 500–600 °C (932–1112 °F; 773–873 K) dengan udara membentuk barium peroksida, yang terurai di atas 700 °C (1292 °F; 973 K) dengan melepaskan oksigen:
Barium sulfat pertama kali diaplikasikan sebagai zat radiokontras dalam pencitraan sinar-X sistem pencernaan pada tahun 1908.
Toksisitas Barium
Data toksikologi hanya tersedia untuk senyawa, karena reaktivitas logamnya yang tinggi. Senyawa barium yang larut dalam air beracun.
Dalam dosis rendah, ion barium bertindak sebagai stimulan otot, dan dosis yang lebih tinggi mempengaruhi sistem saraf, menyebabkan penyimpangan jantung, tremor, kelemahan, kegelisahan, sesak napas, dan kelumpuhan.
Toksisitas ini mungkin disebabkan oleh pemblokiran saluran kalium oleh ion Ba2+, yang sangat penting agar sistem saraf berfungsi dengan tepat. Organ-organ lain yang rusak akibat senyawa barium yang larut dalam air (yaitu ion barium) adalah mata, sistem kekebalan tubuh, jantung, sistem pernapasan, dan kulit, menyebabkan, misalnya, kebutaan dan sensitisasi.
Barium tidak bersifat karsinogenik dan tidak mengalami bioakumulasi (penimbunan substansi di dalam tubuh suatu organisme).
Debu yang terhirup yang mengandung senyawa barium yang tidak larut dapat menumpuk di paru-paru, menyebabkan kondisi benigna yang disebut baritosis.
Sulfat yang tidak larut tidak beracun dan tidak diklasifikasikan sebagai barang berbahaya dalam peraturan transportasi.
Untuk menghindari potensi reaksi kimia yang hebat, logam barium disimpan dalam atmosfer argon atau di dalam minyak mineral. Kontak dengan udara dapat berbahaya dan bisa menyebabkan pengapian. Kelembaban, gesekan, panas, percikan api, api, guncangan, listrik statis, serta paparan oksidator dan asam harus dihindari. Apa pun yang mungkin kontak dengan barium harus terbumikan listriknya.
Siapa pun yang bekerja dengan logam ini harus memakai sepatu yang tidak memicu percikan, pakaian karet tahan api, sarung tangan karet, celemek, kacamata pelindung, dan masker gas. Dilarang merokok di wilayah kerja. Pencucian menyeluruh diperlukan setelah penanganan barium.
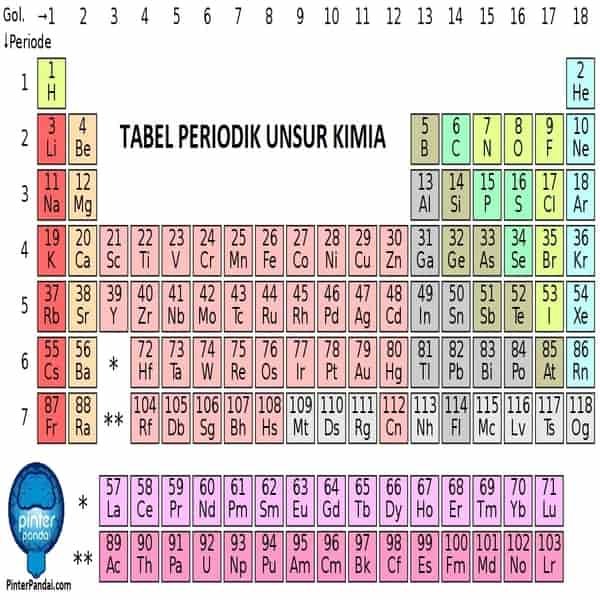
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Kembang Api – Pengertian, Dampak, Bahan Kimia, Pembuatan, Warna
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Cleverly Smart, Royal Society of Chemistry
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing