Belerang
Belerang adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang S dan nomor atom 16.
Fisik Belerang
Belerang (sulfur) adalah unsur non-logam multivalen, berlimpah, tidak berasa dan tidak berbau. Dalam bentuk alami, belerang berbentuk kristal padat berwarna kuning.
Meskipun belerang terkenal karena baunya busuk, bau ini sebenarnya berasal dari gas hidrogen sulfida (H2S), bukan dari belerang murni. Belerang memiliki kristalografi kompleks.

Isotop
Ada empat isotop stabil belerang termasuk sulfur-32, 33, 34, dan 36. Mayoritas alami belerang adalah belerang-32.
Senyawa Belereang
Asam Sulfat (H2SO4)
Asam sulfat sangat korosif dan reaksi hidrasi dengan air sangat eksotermis. Selalu tambahkan asam ini ke air untuk mengencerkannya, jangan sekali-kali menuang air ke dalam asam sulfat. Asam sulfat juga sangat kuat sebagai dehidrator dan harus dilakukan dengan sangat hati-hati. Asam sulfat murni mempunyai sifat hantaran listrik yang signifikan sebagai akibat sifat swaionisasi menurut persamaan reaksi :
2H2SO4(l) → H2O(H2SO4) + H2S2O7(H2SO4)
H2O(H2SO4) + H2SO4(l) H3O+ (H2SO4) + HSO4– (H2SO4)
H2O(H2SO4) + H2S2O7(H2SO4) → H3O+ (H2SO4) + HS2O7– (H2SO4)
Sifat korosif asam sulfat dapat merusak benda-benda dari logam, karena logam akan teroksidasi baik dengan asam sulfat encer maupun pekat. Contoh reaksi logam dengan asam sulfat encer,
Mg(s) + H2SO4(aq) → MgSO4(aq) + H2(g)
Reaksi logam dengan asam sulfat pekat,
Mg(s) + H2SO4(aq) → MgSO4(aq) + SO2(g) + H2O(l)
Asam sulfat pekat dapat menarik molekul air dari senyawa-senyawa lain dalam proses dehidrasi. Ketika asam sulfat pekat diteteskan ke kertas tissue, akan terjadi dehidrasi dan kertas itu menjadi gosong, warnanya menjadi hitam karena terbentuk arang dan berlubang-lubang.
Asam sulfat encer
Asam sulfat encer sering digunakan sebagai suatu asam. Asam sulfat encer adalah asam kuat diprotik membentuk dua anion, ion hidrogen sulfat, H2O4– dan ion sulfat, SO42-, menurut persamaan ionisasi sebagai berikut :
H2SO4(aq)+ H2O(l) → H3O+(aq) + HSO4–(aq)
HSO4–(aq) )+ H2O(l)→ H3O+(aq) + SO42-(aq)
Persamaan keseimbangan pertama terletak jauh lebih menggeser ke arah kanan daripada persamaan keseimbangan ke dua. Jadi spesies yang dominan dalam larutan encer asam sulfat adalah ion hidronium, H3O+ dan ion hidrogen sulfat, HSO4–.
Sejarah Belerang
Belerang sudah diketahui sejak zaman kuno. Budaya kuno di India, Cina, dan Yunani semua tahu tentang belerang. Hal ini bahkan disebut dalam Alkitab sebagai “belerang.” Kadang-kadang dieja “sulfur.”
kimiawan Perancis Antoine Lavoisier yang, pada tahun 1777, membuktikan belerang yang merupakan salah satu dari unsur-unsur dan bukan senyawa.
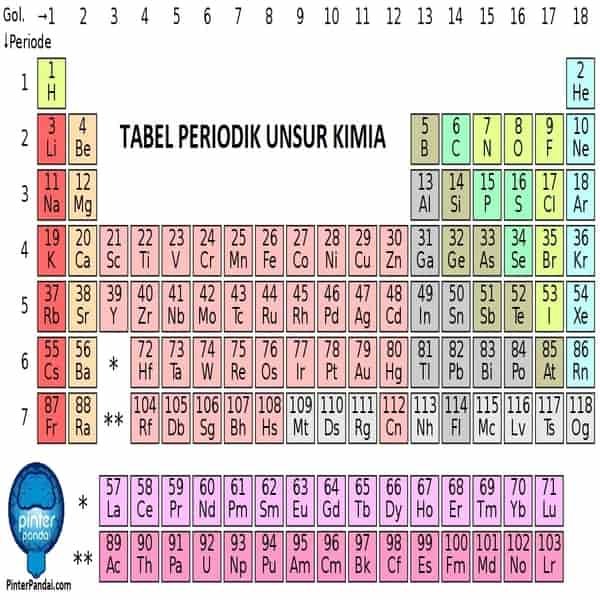
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Manfaat Emas Dalam Pengobatan Kesehatan Medis
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, Libretexts
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya