Boron
Boron adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang B dan nomor atom 5.
Kegunaan Boron
Boron sering digunakan sebagai penyala bahan bakar roket dan pemicu api dalam teknik.
Di lingkungan, boron terdapat pada bubuk pembersih dan pengawet boraks. Boraks banyak digunakan dalam pembuatan pembersih. Boraks oksida juga sering dugunakan dalam pabrik gelas borosilikat (pada Pyrex). Boraks oksida dapat membuat gelas tahan panas dan lebih kuat. Fiberglas dalam tekstil juga menggunakan bahan dasar borosilikat. Boron digunakan dalam pembuatan kembang api untuk memberikan warna hijau.
Isotop boron 10 dapat menyerap neutron dengan baik. Karena sifatnya ini, dalam ilmu kimia isotop boron 10 digunakan dalam mengontrol reaktor nuklir, sebagai tameng untuk radiasi nuklir dan juga dapat digunakan pula dalam instrument untuk mendeteksi keberadaan neutron pada sample.
Boron terutama ditemukan di sayuran dan buah-buahan, sedangkan produk daging mengandung boron dalam jumlah sedikit. Berikut adalah makanan yang kaya akan boron:
- Sayuran seperti tomat dan kacang panjang.
- Buah-buahan seperti anggur, apel, pir, kismis dan kiwi.
- Kacang-kacangan seperti almond dan kacang tanah.

Sejarah Boron
Pada tahun 1808, Louis Josef Gay Lusac dan Louis Jacques Thenard melakukan penelitian di Paris. Pada saat yang sama, Sir Humpry Davy juga melakukan penelitian yang sama di London. Mereka secara independen (masing-masing) mengekstrak unsur kimia boron dengan cara memanaskan borax dengan logam kalium.
Kenyataannya mereka berhasil memproduksi unsur yang hampir mustahil untuk diperoleh pada masa itu, zat ini disebut boron. Pada tahun 1892 Henri Moissan berhasil melakukan ekstraksi boron dengan lebih murni.
Reaksi-Reaksi Boron
Reaksi boron dengan Air
Boron tidak dapat bereaksi dengan air pada kondisi normal.
Reaksi antara boron dengan halogen
Boron dapat bereaksi dengan
halogen dan fluorine F2, clorin, dan blromin, untuk membentuk trihalida, contohnya; Boron(III) Fluoride BF3, Boron (III) Bromida BBr3.
Raksi boron dengan udara
Reaksi antara boron dengan udara
tergantung pada kristalitas dari sampel boron, temperatur dan ukuran partikel, dan kemurnian dari boron tersebut. Se3bagian besar boron tidak akan bereaksi dengan udara pada temperatur ruang. Namun pada temperatur yang lebih tinggi, boron akan bereaksi dengan udara berdasarkan persamaan reaksi:
4B + 3O2(g) → 2B2O3(s)
Reaksi Boron dengan asam

Isotop Boron
Isotop Boron terstabil
| Isotop | Kelimpahan | Waktu paruh (t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 10B | 19.9(7)%* | 10B stabil dengan 5 neutron | |||
| 11B | 80.1(7)%* | 11B stabil dengan 6 neutron | |||
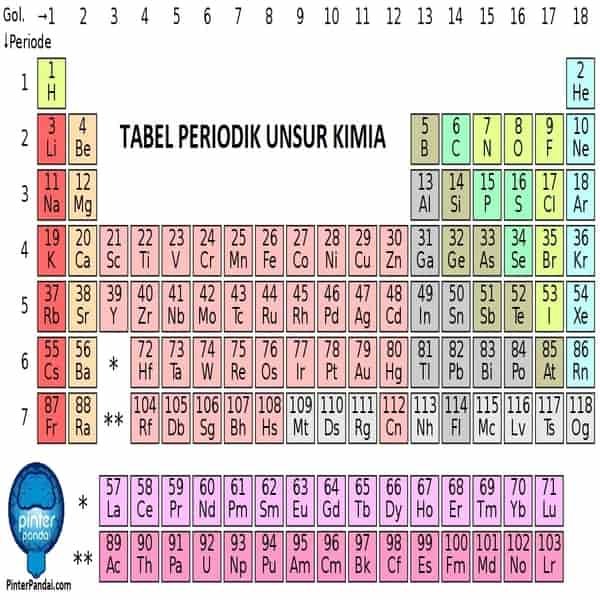
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Manfaat Emas Dalam Pengobatan Kesehatan Medis
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Cleverly Smart, Wikipedia
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing