Kalium
Kalium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang K dan nomor atom 19.
Fisik Kalium
Kalium adalah logam berdensitas paling rendah kedua setelah litium. Ia adalah padatan lunak dengan titik leleh rendah, dan mudah dipotong dengan pisau. Kalium yang baru dipotong berwarna keperakan, tapi mulai muncul noda abu-abu segera saat terpapar udara. Dalam uji nyala api, kalium dan senyawanya memancarkan warna ungu dengan panjang gelombang puncak emisi 766,5 nanometer
Fungsi Kalium Dalam Kehidupan Sehari-Hari
Permintaan terbanyak untuk kalium adalah untuk pupuk. Kalium merupakan bahan penting untuk pertumbuhan tanaman dan ditemukan di banyak tanah. Campuran logam natrium dan kalium (NaK) digunakan sebagai media perpindahan panas. Banyak garam-garam kalium seperti hidroksida, nitrat, karbonat, klorida, klorat, bromida, ioda, sianida, sulfat, kromat dan dikromat sangat penting untuk banyak kegunaan.
Kalium adalah unsur kedelapan atau kesembilan yang paling umum dalam tubuh manusia berdasarkan massa (0,2%), sehingga 60 kg orang dewasa mengandung total sekitar 120 g kalium. Tubuh memiliki kalium kira-kira sebanyak belerang dan klorin, dan hanya kalsium dan fosfor yang lebih banyak (kecuali unsur CHON (en) yang ada di mana-mana). Ion kalium hadir dalam berbagai macam protein dan enzim.

Senyawa Kimia Kalium
Atom kalium netral memiliki 19 elektron, satu lebih banyak daripada konfigurasi gas mulia argon yang sangat stabil. Oleh karena itu dan energi ionisasi pertamanya yang serendah 418,8 kJ/mol, atom kalium lebih cenderung kehilangan elektron terakhir sehingga bermuatan positif daripada mendapatkan satu elektron untuk memperoleh muatan negatif (walaupun ion alkalida bermuatan negatif K− bukan tidak mungkin). Proses ini membutuhkan sangat sedikit energi agar kalium mudah teroksidasi oleh oksigen atmosfer. Sebaliknya, energi ionisasi kedua sangat tinggi (3052 kJ/mol), karena pelepasan dua elektron melanggar konfigurasi elektron gas mulia yang stabil (konfigurasi argon inert). Oleh karenanya, kalium tidak mudah membentuk senyawa dengan keadaan oksidasi +2 atau lebih tinggi.
pembuatan magnesium dari magnesium klorida dengan metode ini menggunakan kalium sebagai reduktor:
Satu-satunya tingkat oksidasi kalium yang umum adalah +1. Logam kalium adalah reduktor kuat yang mudah teroksidasi menjadi kation monopositif, K+. Sekali teroksidasi, ia sangat stabil dan sulit untuk direduksi kembali menjadi logamnya.
Kalium hidroksida mudah bereaksi dengan karbon dioksida menghasilkan kalium karbonat dan digunakan untuk menghilangkan gas renik dari udara. Secara umum, senyawa kalium memiliki kelarutan yang sangat tinggi dalam air, karena energi hidrasi ion K+ yang tinggi. Ion kalium tidak berwarna dalam air dan sangat sulit diendapkan; metode presipitasi yang mungkin termasuk reaksi dengan natrium tetrafenilborat, asam heksakloroplatinat dan natrium. kobaltinitrit.
Isotop Kalium
Terdapat 24 isotop kalium yang diketahui, yang tiga di antaranya terjadi secara alami: 39K (93,3%), 40K (0,0117%), dan 41K (6,7%). 40K yang terjadi secara alami memiliki waktu paruh 1,250×109 tahun. Ia meluruh menjadi 40Ar yang stabil melalui penangkapan elektron atau emisi positron (11,2%) atau menjadi 40Ca yang stabil melalui peluruhan beta (88,8%).
Peluruhan 40K menjadi 40Ar adalah dasar metode umum untuk penanggalan batuan. Metode penanggalan K-Ar konvensional bergantung pada asumsi bahwa batuan tidak mengandung argon pada saat pembentukannya dan bahwa semua argon radiogenik selanjutnya (40Ar) dipertahankan secara kuantitatif. Mineral diberi tanggal dengan pengukuran konsentrasi kalium dan jumlah 40Ar radiogenik yang telah terakumulasi. Mineral yang paling cocok untuk diberi penanggalan termasuk biotit, muskovit, hornblende metamorf, dan feldspar vulkanik; sampel batuan utuh dari aliran vulkanik dan instrusif dangkal juga bisa diberi tanggal jika tidak dialterasi.
Selain untuk penanggalan, isotop kalium telah digunakan sebagai pelacak dalam studi pelapukan dan studi siklus nutrisi karena kalium adalah makronutrien yang dibutuhkan untuk kehidupan.
40K terdapat dalam kalium alami (dan sehingga terdapat dalam beberapa substitusi garam komersial) dalam jumlah yang cukup, maka kantong besar pengganti tersebut dapat digunakan sebagai sumber radioaktif untuk demonstrasi di kelas. 40K adalah radioisotop dengan kelimpahan terbesar di dalam tubuh. Pada hewan dan manusia sehat, 40K merupakan sumber radioaktivitas terbesar, lebih besar daripada 14C sekalipun. Dalam tubuh manusia massa 70 kg, sekitar 4.400 inti 40K meluruh setiap detiknya. Aktivitas kalium alami adalah 31 Bq/g.

Mutiara kalium dalam minyak parafin. Ukuran mutiara besar 0,5 cm.
Sejarah Kalium
Logam kalium pertama kali diisolasi pada tahun 1807 di Inggris oleh Sir Humphry Davy, yang mengisolasinya dari kaustik potas (KOH, kalium hidroksida) dengan elektrolisis leburan KOH dengan tumpukan volta, teknologi yang baru ditemukan. Kalium adalah logam pertama yang diisolasi dengan elektrolisis. Dalam bahasa Inggris, unsur ini disebut potassium.
Kemudian pada tahun yang sama, Davy melaporkan ekstraksi logam natrium dari mineral derivatif (soda api, NaOH atau lindi) dan bukan dari garam tanaman, dengan teknik serupa, menunjukkan bahwa unsur-unsurnya, dan juga garamnya, berbeda.
Meskipun produksi logam kalium dan natrium seharusnya telah menunjukkan bahwa keduanya adalah unsur, perlu beberapa waktu sebelum pandangan ini diterima secara universal.
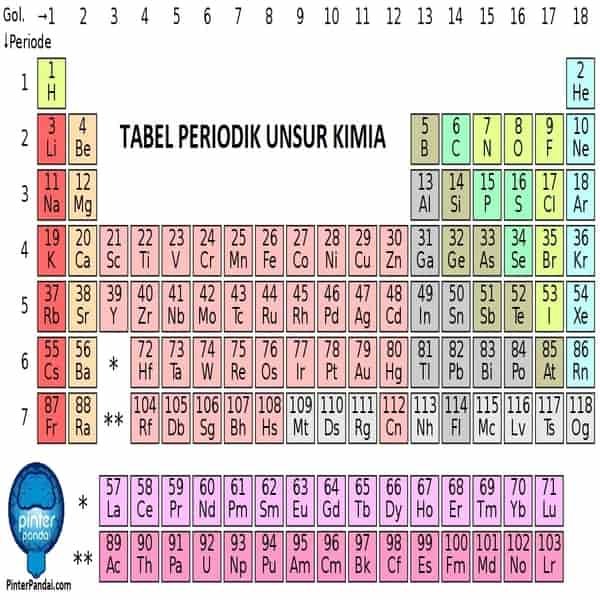
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Manfaat Emas Dalam Pengobatan Kesehatan Medis
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya