Stronsium
Stronsium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Sr dan nomor atom 38. Sebuah logam alkali tanah, strontium adalah unsur logam lunak perak-putih atau kekuningan yang sangat reaktif kimia. logam membentuk lapisan oksida gelap bila terkena udara.
Penggunaan
Digunakan untuk memproduksi kaca (tabung sinar katoda) untuk televisi berwarna. Ini juga digunakan dalam memproduksi magnet keramik ferit dan pemurnian seng.
Kloridanya digunakan dalam manajemen nyeri tulang pada kanker prostat.
Garamnya digunakan dalam flare dan kembang api untuk warna merah tua.
Kloridanya digunakan dalam pasta gigi untuk gigi sensitif.
Oksidanya digunakan untuk meningkatkan kualitas glasir tembikar.
Cat dan plastik ‘glow-in-the-dark’ modern mengandung strontium aluminate.
Isotop 90Sr adalah salah satu penghasil beta berenergi tinggi terbaik yang diketahui. Ini digunakan dalam terapi kanker.
Karakteristik Stronsium
Stronsium adalah logam keperakan divalen dengan warna kuning pucat yang sifat sebagian besar peralihan antara dan mirip dengan kalsium tetangga kelompok dan barium. Hal ini lebih lembut dari kalsium dan lebih sulit daripada barium. Its leleh (777 °C) dan titik didih (1655 °C) poin lebih rendah daripada kalsium (842 °C dan 1757 °C masing-masing); barium terus tren ini penurunan titik leleh (727 °C), tapi tidak di titik didih (2170 °C). Kepadatan Stronsium (2,64 g / cm3) adalah sama antara antara kalsium (1,54 g / cm3) dan barium (3,594 g / cm3). Tiga alotrop Stronsium logam ada, dengan titik transisi pada 235 dan 540 °C.
Potensial elektroda standar untuk Sr2 + / pasangan Sr adalah -2,89 V, sekitar tengah-tengah antara orang-orang dari Ca2 + / Ca (-2,84 V) dan Ba2 + / Ba (-2,92 V) pasangan, dan dekat dengan orang-orang dari logam alkali tetangga.
Stronsium adalah penengah antara kalsium dan barium reaktivitas ke arah air, dengan yang bereaksi pada kontak untuk menghasilkan strontium hidroksida dan gas hidrogen.
Stronsium logam terbakar di udara untuk menghasilkan baik oksida stronsium dan stronsium nitrida, tetapi karena tidak bereaksi dengan nitrogen di bawah 380 °C, pada suhu kamar, membentuk hanya oksida secara spontan. Selain SrO oksida sederhana, SrO2 peroksida dapat dibuat dengan oksidasi langsung dari logam strontium di bawah tekanan tinggi oksigen, dan ada beberapa bukti untuk Sr superoksida kuning (O2) 2. Strontium hidroksida, Sr (OH) 2, merupakan dasar yang kuat, meskipun tidak sekuat hidroksida barium atau logam alkali.
Karena ukuran besar dari elemen-elemen blok berat, termasuk Stronsium, berbagai macam bilangan koordinasi diketahui, dari 2, 3, atau 4 sampai ke 22 atau 24 di SrCd11 dan SrZn13. Ukuran besar strontium dan barium memainkan peran penting dalam menstabilkan kompleks Stronsium dengan ligan makrosiklik polidentat seperti eter mahkota: misalnya, sementara 18-crown-6 bentuk kompleks relatif lemah dengan kalsium dan logam alkali, strontium dan barium yang kompleks yang jauh lebih kuat.
Senyawa Organostrontium mengandung satu atau lebih ikatan strontium-karbon. Mereka telah dilaporkan sebagai perantara dalam reaksi Barbier-jenis.
Meskipun Stronsium berada di kelompok yang sama seperti magnesium, dan senyawa organomagnesium sangat umum digunakan di seluruh kimia, senyawa organostrontium tidak sama luas karena mereka lebih sulit untuk membuat dan lebih reaktif. senyawa Organostrontium cenderung lebih mirip dengan organoeuropium atau senyawa organosamarium karena jari-jari ion yang sama dari unsur-unsur (Sr2 + 118 pm; EU2 + 117 pm; SM2 + 122 pm). Sebagian besar senyawa ini hanya dapat disiapkan pada suhu rendah; ligan besar cenderung mendukung stabilitas. Misalnya, strontium dicyclopentadienyl, Sr (C5H5) 2, harus dilakukan dengan langsung bereaksi logam strontium dengan mercurocene atau cyclopentadiene sendiri; menggantikan ligan C5H5 dengan bulkier C5 (CH3) 5 ligan di sisi lain meningkatkan kelarutan, volatilitas senyawa ini, dan stabilitas kinetik.
Karena reaktivitas ekstrim dengan oksigen dan air, unsur ini terjadi secara alami hanya dalam senyawa dengan unsur-unsur lain, seperti di strontianite mineral dan Celestine. Hal ini disimpan di bawah hidrokarbon cair seperti minyak mineral atau minyak tanah untuk mencegah oksidasi; baru terkena logam stronsium cepat berubah warna kekuningan dengan pembentukan oksida.
Logam halus Stronsium bubuk adalah piroforik, yang berarti bahwa itu akan menyala secara spontan di udara pada suhu kamar. garam strontium Volatile memberi warna merah terang untuk api, dan garam-garam ini digunakan dalam kembang api dan dalam produksi flare. Seperti kalsium dan barium, strontium logam larut langsung di amonia cair untuk memberikan solusi biru gelap.
Konsekuensi kesehatan
Senyawa strontium yang tidak larut dalam air dapat menjadi tidak larut dalam air sebagai akibat dari reaksi kimia. Senyawa yang dapat larut lebih mungkin mempengaruhi kesehatan kita daripada senyawa yang tidak dapat larut karena dapat mencemari air minum. Untungnya, konsentrasi dalam air minum secara umum cukup rendah.
Anda dapat terkena sejumlah kecil strontium (radioaktif) dengan menghirup udara atau debu, makan, minum, atau kontak dengan tanah yang mengandungnya. Biasanya paparan melalui makanan atau air.
Konsentrasinya dalam makanan berkontribusi pada konsentrasi strontium dalam tubuh manusia. Makanan yang mengandung strontium tinggi adalah biji-bijian, sayuran berdaun dan produk susu.
Kebanyakan orang memilikinya dalam asupan sedang. Satu-satunya senyawa yang dianggap berbahaya bagi kesehatan, meski dalam jumlah kecil, adalah strontium kromat. Bahaya ini terutama karena kromium beracun yang dikandungnya. Kromatnya diketahui menyebabkan kanker paru-paru, tetapi risiko pemaparannya telah sangat dikurangi dengan prosedur keselamatan perusahaan, sehingga tidak lagi menjadi risiko kesehatan yang signifikan.
Konsumsi strontium konsentrasi tinggi umumnya diketahui tidak berbahaya bagi kesehatan. Hanya ditemukan satu kasus alergi strontium, tetapi tidak ada kasus serupa lainnya. Pada anak-anak, mengonsumsi terlalu banyak strontium dapat menimbulkan risiko karena dapat menyebabkan gangguan pada pertumbuhan tulang.
Ketika konsumsi strontium sangat tinggi dapat menyebabkan gangguan pada perkembangan tulang, tetapi ini hanya terjadi bila konsumsi berada di urutan seribu ppm. Tingkat strontium dalam makanan dan air minum tidak cukup tinggi untuk menyebabkan efek jenis ini.
Stronsium radioaktif mewakili risiko kesehatan yang lebih besar daripada strontium stabil. Ketika konsumsi sangat tinggi, dapat menyebabkan anemia dan kekurangan oksigen dan, pada konsentrasi yang sangat tinggi, bahkan diketahui menyebabkan kanker karena perubahan materi genetik sel.
Dampak lingkungan
Stronsium dalam bentuk unsurnya secara alami ada di lingkungan (batuan, tanah, air, udara). Senyawanya dapat bergerak di lingkungan dengan cukup mudah karena banyak di antaranya yang dapat larut.
Itu selalu hadir di udara sebagai debu hingga tingkat tertentu. Konsentrasinya di udara meningkat oleh aktivitas manusia, seperti pembakaran batu bara dan minyak.
Partikel debu yang mengandung strontium dapat mengendap di permukaan air, tanah dan pada tumbuhan. Ketika partikel tidak mengendap, mereka jatuh kembali ke permukaan bumi selama hujan atau salju turun. Semua strontium berakhir di tanah atau dasar air permukaan, di mana ia bercampur dengan strontium yang sudah ada.
Itu juga bisa menyusup ke air setelah berada di tanah. Hanya sebagian kecil dari strontium dalam air yang berasal dari partikel debu di udara. Sebagian besar strontium di dalam air terlarut, tetapi sebagian tetap tersuspensi, mengakibatkan pembentukan air berlumpur. Sedikit strontium ditemukan dalam air minum.
Jika konsentrasinya di dalam air melebihi konsentrasi biasa, biasanya hal itu disebabkan oleh aktivitas manusia, terutama ketika limbah dibuang langsung ke air.
Konsentrasi yang berlebihan ini juga dapat disebabkan oleh pengendapan debu udara yang bereaksi dengan partikel strontium yang dipancarkan selama proses industri.
Peningkatan konsentrasi tanah juga dapat dipengaruhi oleh aktivitas manusia seperti pembuangan batubara atau abu insinerator. Stronsium dalam tanah larut dalam air, oleh karena itu, ia cenderung merambat lebih dalam di dalam tanah dan bergabung dengan air tanah. Beberapa strontium yang diperkenalkan oleh manusia tidak mencapai air permukaan dan dapat bertahan di tanah selama beberapa dekade.
Karena sifatnya, beberapa di antaranya dapat diambil oleh ikan, sayuran, ternak, dan hewan lainnya.
Salah satu isotop strontium adalah radioaktif. Isotop ini secara apriori tidak hadir secara alami di lingkungan. Itu ada karena manusia: uji coba bom nuklir, kebocoran penyimpanan radioaktif. Satu-satunya cara untuk menurunkan konsentrasi isotop ini adalah peluruhan radioaktif menjadi zirkonium yang stabil.
Konsentrasi strontium radioaktif di lingkungan relatif rendah, dan partikel-partikel tersebut selalu berakhir di tanah atau di dasar laut, di mana mereka bercampur dengan partikel strontium lainnya. Stronsium radioaktif tidak mungkin berakhir di air minum.
Isotop stronsium terstabil
| Isotop stronsium terstabil | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Penggunaan Stronsium
Mengkonsumsi 75% dari produksi, penggunaan utama untuk strontium di kaca untuk tabung sinar televisi berwarna katoda, di mana ia mencegah emisi sinar-X. Aplikasi ini untuk strontium menurun karena CRT digantikan oleh metode display lainnya. Penurunan ini memiliki pengaruh yang signifikan terhadap pertambangan dan pemurnian strontium. Semua bagian dari CRT harus menyerap sinar-X. Di leher dan corong tabung, kaca timbal digunakan untuk tujuan ini, tetapi ini jenis kaca menunjukkan efek browning karena interaksi sinar-X dengan kaca. Oleh karena itu, panel depan terbuat dari campuran kaca yang berbeda dengan strontium dan barium untuk menyerap sinar-X. Nilai rata-rata untuk campuran kaca ditentukan untuk studi daur ulang pada tahun 2005 adalah 8,5% strontium oksida dan 10% barium oksida.
Rasio 87Sr / 86Sr juga telah digunakan untuk menentukan sumber bahan arkeologi kuno seperti kayu dan jagung di Chaco Canyon, New Mexico. rasio 87Sr / 86Sr di gigi juga dapat digunakan untuk melacak migrasi.
Karena Stronsium sangat mirip dengan kalsium, yang tergabung dalam tulang. Semua empat isotop stabil digabungkan, di sekitar proporsi yang sama mereka ditemukan di alam. Namun, distribusi sebenarnya dari isotop cenderung sangat bervariasi dari satu lokasi geografis yang lain. Dengan demikian, menganalisis tulang dari seorang individu dapat membantu menentukan daerah asalnya. Pendekatan ini membantu untuk mengidentifikasi pola migrasi kuno dan asal-usul manusia commingle tetap di situs medan perang pemakaman.
Rasio 87Sr / 86Sr biasanya digunakan untuk menentukan daerah asalnya mungkin dari sedimen di sistem alam, terutama di laut dan lingkungan fluvial. Dasch (1969) menunjukkan bahwa sedimen permukaan Atlantic ditampilkan rasio 87Sr / 86Sr yang dapat dianggap sebagai rata-rata sebagian besar rasio 87Sr / 86Sr dari terranes geologi dari daratan yang berdekatan. Sebuah contoh yang baik dari sistem fluvial-laut yang studi asal Sr isotop telah berhasil digunakan adalah sistem Sungai Nil-Mediterania. Karena usia yang berbeda dari batu-batu yang merupakan mayoritas Biru dan Nil Putih, daerah resapan dari asalnya mengubah sedimen mencapai delta Sungai Nil dan Timur Laut Mediterania dapat dilihat melalui strontium studi isotop. perubahan tersebut climatically dikendalikan di Akhir Kuarter.
Strontium karbonat dan garam strontium lain yang ditambahkan ke kembang api untuk memberikan warna merah tua. Efek yang sama ini mengidentifikasi kation strontium di uji nyala. Fireworks mengkonsumsi sekitar 5% dari produksi dunia. Strontium karbonat digunakan dalam pembuatan magnet ferit keras.
Strontium chloride kadang-kadang digunakan dalam pasta gigi untuk gigi sensitif. Salah satu merek yang populer meliputi 10% dari total strontium chloride hexahydrate berat. Jumlah kecil yang digunakan dalam penyulingan seng untuk menghapus sejumlah kecil kotoran memimpin. Logam itu sendiri memiliki penggunaan yang terbatas sebagai getter, untuk menghilangkan gas yang tidak diinginkan di Vacuums dengan mereaksikan dengan mereka, meskipun barium juga dapat digunakan untuk tujuan ini.
Jam terbaik di dunia adalah jam atom dibuat dengan atom strontium dalam kisi optik.
Radiasi radioaktif Stronsium
89Sr adalah bahan aktif dalam Metastron, radiofarmaka yang digunakan untuk nyeri tulang sekunder untuk kanker tulang metastatik. strontium diproses seperti kalsium oleh tubuh, istimewa memasukkan ke tulang pada situs meningkat osteogenesis. lokalisasi ini berfokus paparan radiasi pada lesi kanker.
90Sr telah digunakan sebagai sumber listrik untuk generator termoelektrik radioisotop (RTG). 90Sr memproduksi sekitar 0,93 watt panas per gram (lebih rendah untuk bentuk 90Sr digunakan dalam RTGS, yang strontium fluoride). Tetapi, 90Sr memiliki sepertiga hidup dan kepadatan rendah dari 238Pu, bahan bakar RTG lain. Keuntungan utama dari 90Sr adalah bahwa hal itu lebih murah daripada 238Pu dan ditemukan dalam limbah nuklir. Uni Soviet dikerahkan hampir 1000 dari RTGS ini di pantai utara sebagai sumber daya untuk mercusuar dan stasiun meteorologi.
Sifat fisika Stronsium
| Sifat fisika | |
|---|---|
| Fase | solid |
| Titik lebur | 1050 K (777 °C, 1431 °F) |
| Titik didih | 1655 K (1382 °C, 2520 °F) |
| Kepadatanmendekati s.k. | 2.64 g/cm3 |
| saat cair, pada t.l. | 2.375 g/cm3 |
| Kalor peleburan | 7.43 kJ/mol |
| Kalor penguapan | 136.9 kJ/mol |
| Kapasitas kalor molar | 26.4 J/(mol·K) |
Tekanan uap
| P (Pa) | 1 | 10 | 100 | 1 k | 10 k | 100 k |
|---|---|---|---|---|---|---|
| at T (K) | 796 | 882 | 990 | 1139 | 1345 | 1646 |
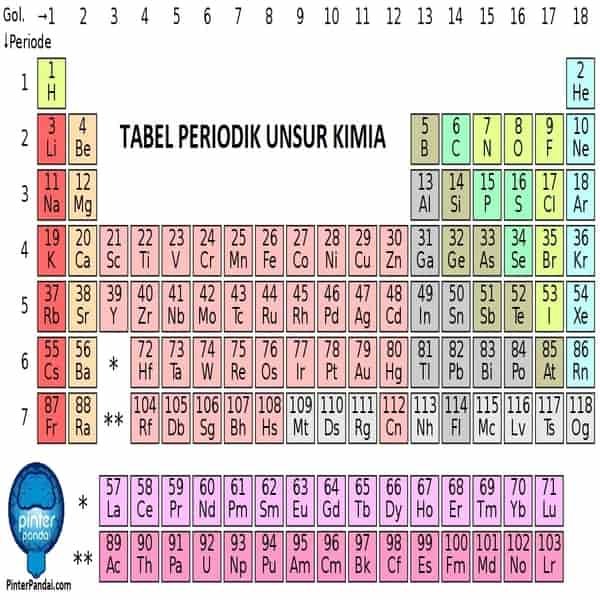
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Bidang-Bidang Matematika: Besaran, Ruang, Perubahan, Struktur, Dasar dan Filsafat, Diskret, Terapan
- Barisan Aritmetika dan Deret Aritmetika
- Quiz gunung tertinggi di Jepang?
- 24 Foto Yang Menunjukkan Mengapa Wisatawan Memilih Kyoto Sebagai Kota Terbaik Di Dunia
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
- Kepalan Tangan Menandakan Karakter Anda – Kepalan nomer berapa yang Anda miliki?
- 7 Cara Untuk Menguji Apakah Dia, Adalah Teman Sejati Anda Atau Bukan BFF (Best Friend Forever)
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Cleverly Smart, Royal Society of Chemistry
Sumber foto: Wikimedia Commons
Penjelasan foto: Strontium unsur kimia sebagai kristal sintetis, disegel di bawah argon dalam ampul kaca, kemurnian (99,95%). Ukuran gambar ca. 3cm * 4,7cm.
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing